Cardiotoxicity as a cause of heart failure with a reduced ejection fraction
Cardiotoxicidad como causa de insuficiencia card├şaca con fracci├│n de eyecci├│n reducida
Authors: Eduardo S├ínchez Mart├şnez
Coauthors: Claudia Moreno Navarro, Teresa Martinez-Carbonell Baeza, Carmen González Tudela, Christian Ruzafa Martinez, Mariano Gambin Arronoz, Jose Garcia Flores, Gonzalo Rocha De Lossada, Jose Javier Tercero Fajardo, Beatriz Castillo Guardiola
Keywords: Chemotherapy. Cancer. Secondary effects. Chronic heart failure. Reduced ejection fraction
Keywords: Quimioterapia. C├íncer. Efectos secundarios. Insuficiencia card├şaca. Fracci├│n de eyecci├│n reducida
Abstract: Chemotherapy use in onchological patients and the continuous advance in this field have caused important survival rates rise and pathologies regarding secondary effects of this treatment likewise. A case of a patient who suffered breast cancer at early age is presented, in which surgery, chemo and radio where used. After 20 years, she suffered from minimum effort dyspnea when she was diagnosed with chronic heart failure with severe reduced ejection fraction secondary to the use of anthracyclines. After the diagnosis, an optimal treatment based on suppressors sodium glucose cotransporter, beta blockers, mineralocorticoids antagonist, aldosterone receptor type 2 antagonists and neprylisin inhibitors was started and lead to the recovering from the acute process and restoring the heart function.
Abstract : El uso de quimioterapia en pacientes oncol├│gicos y el continuo avance de la medicina en este campo, ha provocado un aumento considerable de la supervivencia y por consiguiente de enfermedades relacionadas con los efectos secundarios derivados del tratamiento. Se presenta el caso de una paciente que padeci├│ c├íncer de mama a una edad temprana donde se emple├│ tras la cirug├şa, quimio y radioterapia. Al cabo de 20 a├▒os comienza con disnea de m├şnimos esfuerzos diagnostic├índose una insuficiencia card├şaca severa con fracci├│n de eyecci├│n reducida (ICFEr) secundaria al empleo de antraciclinas. Tras realizar un amplio diagn├│stico diferencial del cuadro, se inicia tratamiento ├│ptimo con inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT2), betabloqueantes (B-bloqueantes), antagonistas mineralcorticoides (ARM), antagonistas del receptor de aldosterona tipo 2 (ARA II) e inhibidores de la neprilesina, recuper├índose del cuadro agudo y restableci├ęndose la funci├│n del coraz├│n.
15-03-2023
Eduardo S├ínchez Mart├şnez
0 Comments
| Citation: Eduardo S├ínchez Mart├şnez, Claudia Moreno Navarro, Teresa Martinez-Carbonell Baeza, Carmen Gonz├ílez Tudela, Christian Ruzafa Martinez, Mariano Gambin Arronoz, Jose Garcia Flores, Gonzalo Rocha De Lossada, Jose Javier Tercero Fajardo, Beatriz Castillo Guardiola. Cardiotoxicidad como causa de insuficiencia card├şaca con fracci├│n de eyecci├│n reducida. https://doi.org/10.24175/sbd.2023.000003 |
| Received: March 15, 2023 Accepted: March 17, 2023 Published: March 17, 2023 |
| Copyright: © 2023 Scientific Editions and Assessment. This is an open access article distributed under the terms of the Creative Commons Attribution License (CC BY-NC), which allows, distribution, reproduction in any medium, provided the original author and source are credited and non-commercial use. |
| Funding: I certify that no funding has been received for the conduct of this study and/or preparation of this manuscript. |
| Conflicts of Interest: I have no conflicts of interest to declare |
Cardiotoxicidad como causa de insuficiencia cardíaca con fracción de eyección reducida
Cardiotoxicity as a cause of heart failure with a reduced ejection fraction
Eduardo Sánchez Martínez1, Beatriz Castillo Guardiola2, Carmen Gónzalez Tudela1, Christian Ruzafa Martínez4, Claudia Moreno Navarro1, Gonzalo Rocha de Lossada3, José García Flores4, José Javier Tercero Fajardo5, Mariano Gambín Arróniz4, Teresa Martínez-Carbonell Baeza1.
Servicio de Medicina Interna; Hospital Universitario Morales Meseguer; Murcia1, Servicio de Medicina Interna; Hospital del Altiplano; Yecla; Murcia2, Servicio de Medicina Interna; Hospital Universitario Virgen de la Arrixaca; Murcia3, Servicio de Medicina Interna; Hospital Universitario Reina Sofía; Murcia4, Servicio de Cardiología; Hospital Universitario Virgen de la Arrixaca; Murcia5
Palabras clave: Quimioterapia, cáncer, efectos secundarios, insuficiencia cardíaca, fracción de eyección reducida.
Resumen
El uso de quimioterapia en pacientes oncológicos y el continuo avance de la medicina en este campo, ha provocado un aumento considerable de la supervivencia y por consiguiente de enfermedades relacionadas con los efectos secundarios derivados del tratamiento. Se presenta el caso de una paciente que padeció cáncer de mama a una edad temprana donde se empleó tras la cirugía, quimio y radioterapia. Al cabo de 20 años comienza con disnea de mínimos esfuerzos diagnosticándose una insuficiencia cardíaca severa con fracción de eyección reducida (ICFEr) secundaria al empleo de antraciclinas. Tras realizar un amplio diagnóstico diferencial del cuadro, se inicia tratamiento óptimo con inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT2), betabloqueantes (B-bloqueantes), antagonistas mineralcorticoides (ARM), antagonistas del receptor de aldosterona tipo 2 (ARA II) e inhibidores de la neprilesina, recuperándose del cuadro agudo y restableciéndose la función del corazón.
Keywords: Chemotherapy, cancer, secondary effects, chronic heart failure, reduced ejection fraction.
Abstract
Chemotherapy use in onchological patients and the continuous advance in this field have caused important survival rates rise and pathologies regarding secondary effects of this treatment likewise. A case of a patient who suffered breast cancer at early age is presented, in which surgery, chemo and radio where used. After 20 years, she suffered from minimum effort dyspnea when she was diagnosed with chronic heart failure with severe reduced ejection fraction secondary to the use of anthracyclines. After the diagnosis, an optimal treatment based on suppressors sodium glucose cotransporter, beta blockers, mineralocorticoids antagonist, aldosterone receptor type 2 antagonists and neprylisin inhibitors was started and lead to the recovering from the acute process and restoring the heart function.
Introducción
La insuficiencia cardíaca (IC) es un síndrome clínico caracterizado por síntomas típicos (disnea, edemas, astenia...) que debe acompañarse de signos, como presión venosa yugular elevada, crepitantes pulmonares, edema periférico, entre otros; causado por una anomalía cardíaca estructural y/o funcional que produce una disminución del gasto cardíaco y/o elevación de las presiones intracardíacas.
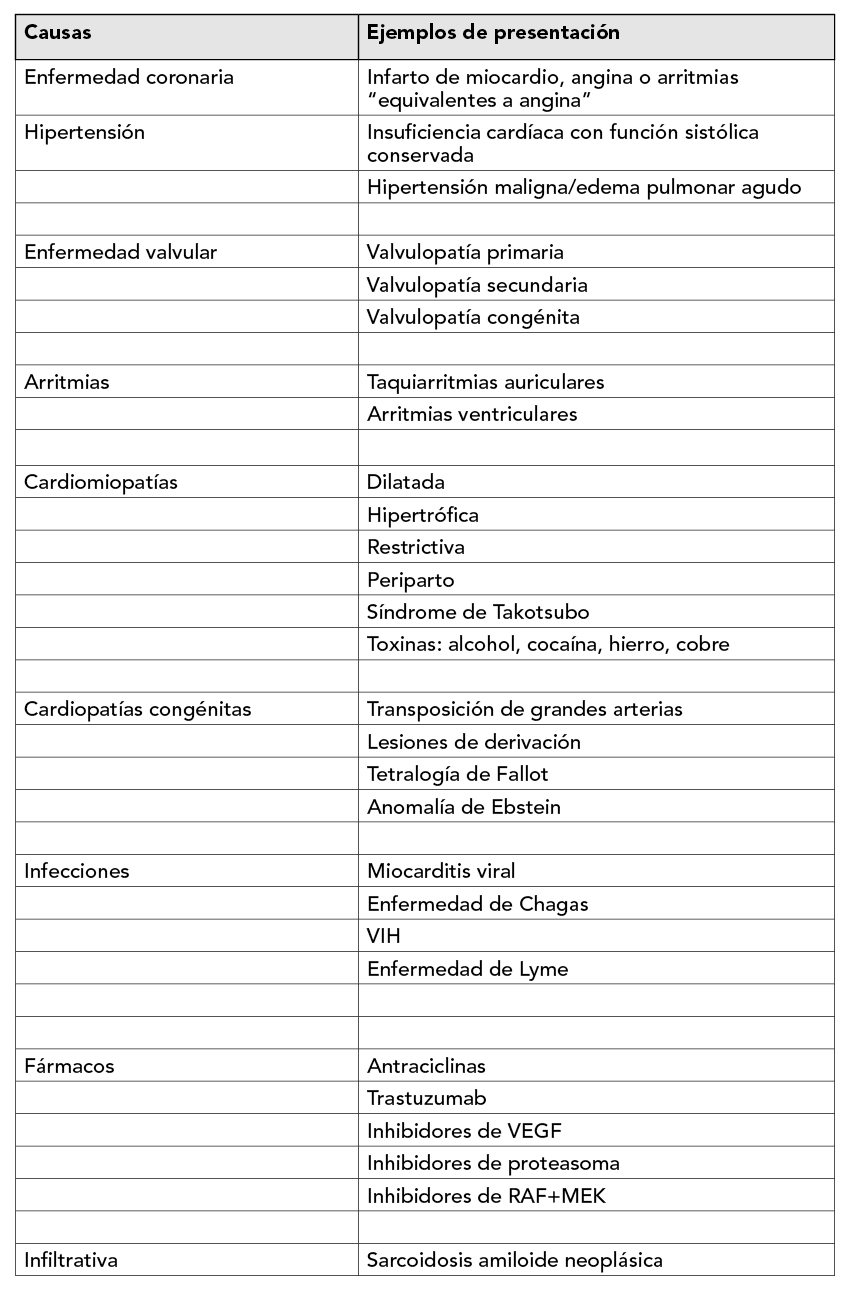
Tradicionalmente, la IC se ha dividido en distintos fenotipos basados en la medición de la fracción de eyección del ventrículo izquierdo (FEVI) (Tabla 1). La identificación de la etiología de la disfunción cardíaca subyacente es fundamental para el diagnóstico de la IC, ya que la afección específica puede determinar el tratamiento. La etiología global de la IC es muy variada (Tabla 2) y aunque la causa más frecuente es la enfermedad coronaria y la hipertensión arterial (HTA)1, se debe realizar un amplio diagnóstico diferencial sirviéndose de las distintas pruebas complementarias para alcanzar un diagnóstico definitivo y tratar en consecuencia.
Nuestro caso versa sobre una mujer de 60 años sin alergias medicamentosas conocidas, que como factores de riesgo cardiovascular presenta dislipemia (DLP), obesidad grado I con IMC 28 kg/m2 y prediabetes. Además, padece de anemia ferropénica crónica secundaria a un mioma uterino, en seguimiento por ginecología. En el año 2002 fue diagnosticada de un carcinoma ductal de mama izquierda que se trató con mastectomía radical, 4 ciclos de antraciclinas y radioterapia, encontrándose en remisión completa en el momento actual. Como antecedentes familiares tiene una madre con cáncer de mama y un abuelo paterno fallecido de infarto agudo de miocardio.
En cuanto al tratamiento crónico toma atorvastatina 10 mg un comprimido por la noche y sulfato de hierro 105 mg un comprimido en ayunas a meses alternos.
El cuadro de la paciente comienza con una disnea progresiva hasta hacerse de moderados/pequeños esfuerzos que la lleva a acudir a urgencias. En un primer momento presenta dificultad para subir un piso de escalera y caminar en pendiente, y progresivamente continúa con disnea incluso al caminar por el domicilio. Además, refiere mal descanso nocturno, con crisis de ortopnea, sudoración, nicturia y ligeros edemas en miembros inferiores. Niega dolor torácico, palpitaciones, síncope, fiebre u otros síntomas acompañantes. En urgencias la paciente se encuentra hemodinámicamente estable, la auscultación cardiopulmonar es rítmica con soplo sistólico en foco mitral III/VI y con crepitantes en ambos campos pulmonares hasta campos medios. El abdomen es ligeramente doloroso a la palpación en hipocondrio derecho sin claros signos de irritación peritoneal. Miembros inferiores con edemas localizados en el tercio distal de ambas piernas sin signos de trombosis venosa profunda.
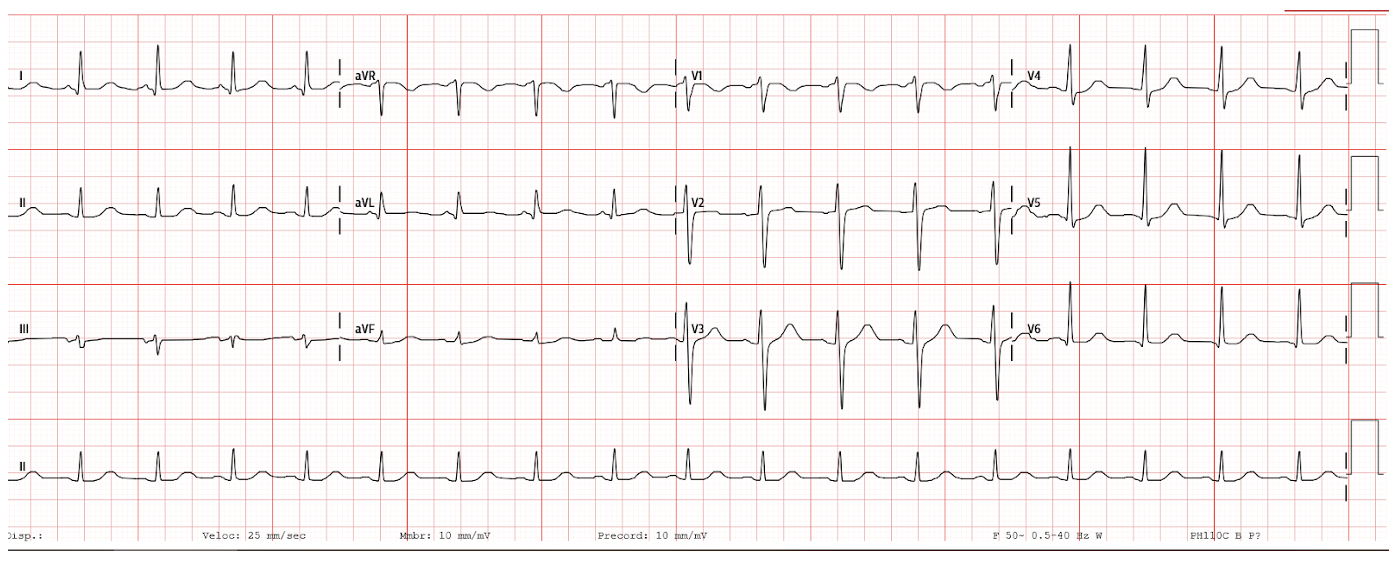
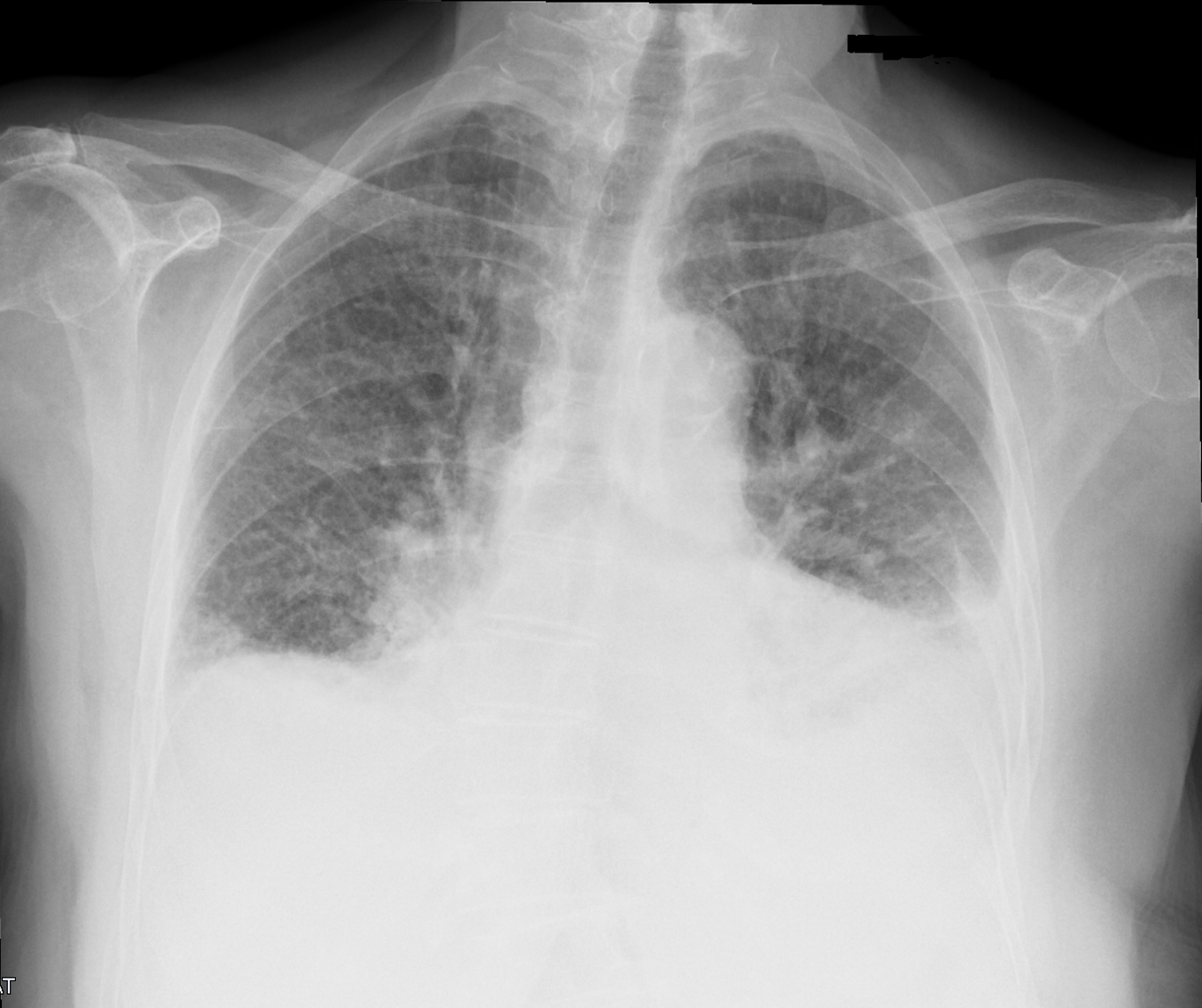
Se realiza electrocardiograma (Figura 1), radiografía de tórax (Figura 2) junto con una analítica básica destacando una creatinina sérica (Cr) de 1.8 mg/dL (niveles normales 0.70 - 1.30 mg/dL) con filtrado glomerular (FG) de 39 ml/min, troponina T seriada de 29 y 31 ng/L (niveles normales 2-50 ng/L), NT-proBNP 4500 pg/mL (niveles normales 0-125 pg/mL), hemoglobina 10.1 g/dl (niveles normales 12.5-17.0 g/dl), resto de la analítica anodina. Ante el cuadro de insuficiencia cardíaca aguda descompensada sin claro cuadro desencadenante, se decide ingresar a la paciente a cargo de medicina interna para realizar estudio y seguimiento.
En planta de hospitalización se continúa con tratamiento diurético iniciado desde urgencias y se realizan pruebas complementarias para ver la causa de la insuficiencia cardíaca de novo. Se realiza en una ecocardiografía donde presenta ventrículo izquierdo moderadamente dilatado con disfunción sistólica severa (FEVI 30%) por hipocinesia global. Insuficiencia mitral (IM) moderada-severa central de aspecto funcional por dilatación del anillo. Insuficiencia tricuspídea ligera con PSAP estimada de 30mmHg, sin derrame pericárdico.
Además, se realiza analítica completa donde destacaría Cr 1.5 mg/dL, LDL 90 mg/dl, Hba1c 6.9%, Nt pro BNP 2500 pg/mL, hemograma con Hb 10.8 g/dl, VCM 80 fl, Hto 23%, 350.000 plaquetas. Ante los resultados de la ecocardiografía, se decide realizar RMN cardíaca donde se objetiva miocardiopatia dilatada no isquémica sin fibrosis con FEVI reducida. Tras las pruebas complementarias se realiza el diagnóstico definitivo de miocardiopatía dilatada secundaria a toxicidad tardía por antraciclinas.
La paciente durante su estancia en planta va mejorando progresivamente del cuadro, se continúa tratamiento con furosemida, además el segundo día se inicia espironolactora 25 mg, al tercero sacubitrilo/valsartán 24-26 mg y al quinto bisoprolol 2.5 mg. Se va subiendo el tratamiento hasta alcanzar la máxima dosis tolerada siendo la misma furosemida 20 mg un comprimido en desayuno, bisoprolol 2.5 mg en desayuno y cena, espironolactona 25 mg un comprimido en desayuno, empaglifozina 10 mg un comprimido en desayuno, sacubitril/valsartán 24/26 mg un comprimido en desayuno y cena. La paciente tiene seguimiento telefónico y presencial continuado con buena evolución, permitiendo retirar furosemida y aumentar dosis de sacubitrilo/valsartán hasta 49/51 mg y espironolactona 50 mg. A los 6 meses, se repite el ecocardiograma con dilatación de VI ligera, mejoría de función sistólica, con FEVI del 53% e IM ligera. Además, a nivel analítico presenta mejoría de la función renal con Cr 0.88 mg/dl, NT-proBNP 561 pg/mL, Hba1c 6.3%.
Discusión
Sabemos que la IC es un problema de primer orden, afecta a más de 26 millones de personas en el mundo y que es una causa importante de morbilidad y gasto sanitario. Además, se asocia con reducciones sustanciales de la calidad de vida y una alta carga asistencial. Se estima que, en los países desarrollados, hasta 1 de cada 5 personas desarrollará insuficiencia cardíaca a lo largo de su vida siendo además la principal causa de hospitalización en personas mayores de 65 años.
En este contexto, es importante conocer el papel de las antraciclinas como parte de los regímenes quimioterapéuticos actuales, cuyo uso lleva adheridos efectos no deseados como la toxicidad cardiológica2. Las antraciclinas pueden producir la lesión de los cardiomiocitos dando lugar al desarrollo de disfunción ventricular izquierda e insuficiencia cardíaca3. Entre los factores de riesgo para cardiotoxicidad se incluyen edad > 65 años o < 18 años, mujer, mayor dosis acumulada de fármaco, enfermedad cardíaca preexistente, hipertensión arterial, ascendencia afroamericana, insuficiencia renal, exposición concomitante a radiación y/o trastuzumab, sobrecarga de hierro y factores genéticos2,3. El mecanismo por el que las antraciclinas producen cardiotoxicidad tiene varias hipótesis, desconociéndose el mecanismo exacto. Se piensa que pueden generar especies reactivas de oxígeno que causan peroxidación lipídica de la membrana celular de los cardiomiocitos, y por lo tanto provocando su lesión. Por otra parte, se cree que se inhibe la topoisomerasa IIβ, lo que puede provocar la activación de las vías de muerte celular y la inhibición de la biogénesis mitocondrial de los cardiomiocitos4.
La toxicidad por antraciclinas puede ocurrir al inicio del tratamiento e incluso hasta varios años después de la finalización del mismo4. El dexrazoxano, los inhibidores del sistema renina-angiotensina-aldosterona, y los betabloqueantes, se han propuesto como fármacos para prevenir la cardiotoxicidad inducida por antraciclinas, no obstante, no se ha establecido claramente un tratamiento preventivo, ya que no hay estudios con resultados consistentes4. La mejora de la supervivencia de los pacientes con cáncer y el conocimiento sobre la cardiotoxicidad de las antraciclinas ha llevado a una mayor vigilancia de los sobrevivientes de cáncer tratados con estos fármacos para una intervención temprana y tratar la insuficiencia cardíaca de acuerdo con las directrices actuales3.
En cuanto al tratamiento de la ICFEr, desde hace unos años se han descubierto nuevas moléculas que han mejorado considerablemente tanto la reducción de ingresos hospitalarios como la mortalidad. Fue sobre mediados de 2014 cuando se empezó a hablar sobre un nuevo fármaco, el sacubitrilo (inhibidor de la neprilesina) el cual supuso un gran avance consiguiendo una reducción de un 20% el riesgo de muerte cardiovascular (CV), un descenso de hasta el 21% el número de primeras hospitalizaciones por IC, y una bajada de un 16% el riesgo de mortalidad5.
En los últimos años ha habido otro hito importante desde el punto de vista del tratamiento de la IC con el desarrollo de los iSGLT2, fármacos desarrollados en un primer momento con otros objetivos (estudio de efectos cardiovasculares de mortalidad y morbilidad en diabéticos tipo 2) pero que ya en los estudios pivotales demostraron sus grandes beneficios no solo a nivel glucémico sino también a nivel renal, metabólico y cardíaco suponiendo una auténtica revolución en la medicina moderna.
Estos fármacos han demostrado ser útiles no solo en pacientes diabéticos sino en todo tipo de enfermos, teniendo unos resultados muy beneficiosos desde el punto de vista CV y renal. Fue sobre 2020 cuando se realizó un estudio diseñado específicamente con el objetivo de valorar los efectos de mortalidad cardiovascular y hospitalizaciones en pacientes con ICFEr obteniéndose una reducción de hasta el 25% en hospitalizaciones por IC o muerte CV, una reducción de hasta el 30% en hospitalizaciones y un retraso en el descenso del filtrado glomerular comparado con placebo6. Además, se vio que estos resultados eran bastante similares tanto en pacientes diabéticos como no diabéticos.
Bibliografía
1. He J, Ogden LG, Bazzano LA, et al. Risk factors for congestive heart failure in US men and women: NHANES I epidemiologic follow-up study. Arch Intern Med 2001; 161:996.
2. Narezkina A, Nasim K. Anthracycline Cardiotoxicity: One step closer to reversing the irreversible. Circulation: Heart Failure. 15 Mar 2019; vol. 12 (3): 1-3.
3. Henriksen PA. Anthracycline cardiotoxicity: an update on mechanisms, monitoring and prevention. Heart 2018;104:971-977.
4. Saleh Y, Abdelkarim O, Herzallah K, Abela GS. Anthracycline-induced cardiotoxicity: mechanisms of action, incidence, risk factors, prevention, and treatment. Heart Fail Rev. 2021 Sep;26(5):1159-1173.
5. McMurray JJ, Packer M, Desai AS, et al. PARADIGM-HF Investigators and Committees. Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med. 2014 Sep 11;371(11):993-1004. doi: 10.1056/NEJMoa1409077. Epub 2014 Aug 30. PMID: 25176015.
6. Packer M, et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med. 2020;383(15):1413-24