Rapidly embolizing intraventricular thrombus formation in dilated cardiomyopathy due to late cardiotoxicity during oligosymptomatic SARCOV-2
Trombo intraventricular embolizante de rápida formación en miocardiopatía dilatada por cardiotoxicidad tardía durante SARCOV-2 oligosintomático
Authors: Noelia Bouzas Cruz
Coauthors: Ana Román Rego, Mauro Trincado Ave, Antía de La Fuente Rey, Federico García-Rodeja Arias, Iván Fernandez Castro, Miguel Franco Álvarez, Clara Casar Cocheteux, Adela Lama López, Rocío Prado Álvarez, Mariño Fernandez Cambeiro, Ariadna Andrade Piña, Manuel Martínez Cereijo
Keywords: Cardio-oncology. Cardiotoxicity. SARSCov-2. Covid-19. Coronavirus-19. Left intraventricular thrombus. Non-ischemic dilated cardiomyopathy
Keywords: Cardio-oncología. Cardiotoxicidad. SARSCov-2. Covid-19. Coronavirus-19. Trombo intraventricular izquierdo. Miocardiopatía dilatada no siquémica
Abstract: Cardio-oncology and Covid-19 are two increasingly topical pathologies. A frequent form of the former is non-ischemic dilated cardiomyopathy, which, like coronavirus infection, is associated with a risk of increased interventricular thrombi. Such thrombi are a potentially fatal problem whose management has not yet been studied in depth, forcing the clinician on many occasions to make decisions without quality evidence to support them. We present a case that combines all these problems.
Abstract : La cardio-oncología y el Covid-19 son dos patologías de creciente actualidad. Una forma frecuente de la primera es la miocardiopatía dilatada no isquémica, que al igual que la infección por coronavirus se asocia con un riesgo de trombos interventriculares aumentados. Dichos trombos son un problema potencialmente mortal cuyo manejo todavía no se ha estudiado en profundidad, obligando al clínico en muchas ocasiones a tomar decisiones sin una evidencia de calidad que lo respalde. Se presenta un caso que combina todas estas problemáticas.
16-03-2023
Noelia Bouzas Cruz
0 Comments
| Citation: Noelia Bouzas Cruz, Ana Román Rego, Mauro Trincado Ave, Antía de La Fuente Rey, Federico García-Rodeja Arias, Iván Fernandez Castro, Miguel Franco Álvarez, Clara Casar Cocheteux, Adela Lama López, Rocío Prado Álvarez, Mariño Fernandez Cambeiro, Ariadna Andrade Piña, Manuel Martínez Cereijo. Trombo intraventricular embolizante de rápida formación en miocardiopatía dilatada por cardiotoxicidad tardía durante SARCOV-2 oligosintomático. https://doi.org/10.24175/sbd.2023.000010 |
| Received: March 16, 2023 Accepted: March 17, 2023 Published: March 17, 2023 |
| Copyright: © 2023 Scientific Editions and Assessment. This is an open access article distributed under the terms of the Creative Commons Attribution License (CC BY-NC), which allows, distribution, reproduction in any medium, provided the original author and source are credited and non-commercial use. |
| Funding: |
| Conflicts of Interest: |
Trombo intraventricular embolizante de rápida formación en miocardiopatía dilatada por cardiotoxicidad tardía durante SARCOV-2 oligosintomático
Rapidly embolizing intraventricular thrombus formation in dilated cardiomyopathy due to late cardiotoxicity during oligosymptomatic SARCOV-2
Noelia Bouzas Cruz, Ana Román Regó, Mauro Trincado Ave, Antía de La Fuente Rey, Federico García-Rodeja Arias, Iván Fernandez Castro, Miguel Franco Álvarez, Clara Casar Cocheteux, Adela Lama López, Rocío Prado Álvarez, Mariño Francisco Fernandez Cambeiro, Ariadna Helena Andrade Piña, Manuel Martínez Cereijo.
CHUS, Complejo Hospitalario Universitario De Santiago de Compostela
DOI: 10.24175/sbd.2023.000010
Palabras clave: Cardiooncología, cardiotoxicidad, SARSCov-2, Covid-19; coronavirus-19, Trombo intraventricular izquierdo, miocardiopatía dilatada no siquémica.
Resumen
La cardiooncología y el Covid-19 son dos patologías de creciente actualidad. Una forma frecuente de la primera es la miocardiopatía dilatada no isquémica, que al igual que la infección por coronavirus se asocia con un riesgo de trombos interventriculares aumentados. Dichos trombos son un problema potencialmente mortal cuyo manejo todavía no se ha estudiado en profundidad, obligando al clínico en muchas ocasiones a tomar decisiones sin una evidencia de calidad que lo respalde. Se presenta un caso que combina todas estas problemáticas.
Keywords: Cardio-oncology, cardiotoxicity, SARSCov-2, Covid-19; coronavirus-19, left intraventricular thrombus, non-ischemic dilated cardiomyopathy.
Abstract
Cardiooncology and Covid-19 are two increasingly topical pathologies. A frequent form of the former is non-ischemic dilated cardiomyopathy, which, like coronavirus infection, is associated with a risk of increased interventricular thrombi. Such thrombi are a potentially fatal problem whose management has not yet been studied in depth, forcing the clinician on many occasions to make decisions without quality evidence to support them. We present a case that combines all these problems.
Introducción
La reciente pandemia por el covid-19 ha supuesto un reto para la atención sanitaria, sometiendo a estas instituciones a la necesidad de atender a un gran volumen de enfermos con unos medios materiales frecuentemente escasos y un conocimiento científico inicialmente muy pobre. Además de sus complicaciones más habituales, la infección por este virus se ha asociado a un estado protrombótico, habiéndose descritos fenómenos trombóticos y tromboembólicos en múltiples territorios. Además, la reacción de la población a la pandemia ha llevado a un retraso de la atención médica, lo que ha condicionado una mayor mortalidad y un mayor número de hospitalizaciones por patologías como la insuficiencia cardíaca o la cardiopatía isquémica.
Otra problemática cada vez más frecuente y que cada día es más estudiada es la cardiotoxicidad del tratamiento quimioterápico, y es que a medida que la esperanza de vida aumenta en aquellos que padecen neoplasias malignas, también aumenta el número de pacientes que requieren una atención cardiológica por las secuelas que estos tratamientos ocasionan.
Respecto a los trombos intraventriculares, se tratan de una complicación con una incidencia de hasta el 15% tras un síndrome coronario agudo con elevación de ST (SCACEST)1, pero su aparición en los pacientes con miocardiopatía dilatada no isquémica es mucho menos frecuente, suponiendo estos pacientes el 21,5% de los casos2. Se trata de un cuadro de elevado riesgo para el paciente, ya que frecuentemente se asocia con tromboembolismos sistémicos. La primera línea de tratamiento es la antiacoagulación2, que puede continuarse a largo plazo de forma segura con antagonistas de la vitamina K (AVK) o anticoagulantes orales de acción directa (NACOs), siendo preciso su mantenimiento al menos los tres-seis primeros meses, pudiendo discontinuarse posteriormente si el trombo ha desaparecido y la FEVI (fracción de eyección ventricular izquierda) es >35%2. No se ha establecido claramente cuál debe ser el tratamiento de elección en el caso de trombos ventriculares resistentes a un primer anticoagulante, existiendo reportes sobre cambio a otro antiacoagulante de otra familia, la adición de un antiagregante e incluso la cirugía3.
Estas cuatro circunstancias confluyen en nuestro caso, que ilustra algunos de los retos más acuciantes de la cardiología contemporánea.
Anamnesis:
Nuestro paciente es una mujer de 68 años sin hábitos tóxicos ni alergias medicamentosas. La paciente presentaba antecedente de hipertensión arterial no tratada. Carecía de antecedentes familiares de muerte súbita, cardiopatía isquémica o insuficiencia cardíaca en familiares de primer y segundo grado. Vida activa, trabajando como oficinista, aunque sin actividad deportiva desde la juventud.
Presentaba una distimia depresiva a tratamiento con sertralina. 10 años antes había padecido un Linfoma no Hodgkin folicular que había respondido favorablemente al tratamiento con ocho ciclos de RCHOP (rituximab, ciclofosfamida, doxorrubicina y vincristina), sin requerir radioterapia. En 2012 presentó un ingreso por una púrpura trombocitopénica idiopática que se había controlado con corticoides, que ya había abandonado. Se encontraba a tratamiento únicamente con sertralina 100 mg c/24 h.
La paciente acudió a la consulta por presentar un cuadro de disnea progresiva de dos meses de evolución, que, aunque incialmente solo se manifestaba al subir cuestas, desde hacía dos semanas también aparecía al deambular en llano. Los últimos tres días diasnea también deambulando por domicilio con ortopnea y disnea paroxística nocturna, por lo que dormía con 2 almohadas. Asimismo, comentaba bendopnea, pero negaba edema de miembros inferiores, síncopes, dolor torácico, fiebre o focalidad infecciosa. Negaba episodios similares en el pasado.
Exploración física
Paciente hipertensa (164/104) con frecuencia cardíaca controlada (71 Lpm).
SatO2 93% con aire ambiente.
Presentaba ingurgitación venosa yugular y reflujo hepatoyugular.
Auscultación pulmonar: crepitantes en bases y campos medios y ligeros sibilantes espiratorios difusos.
Auscultación cardíaca: rítmica y sin soplos.
Abdomen: blando, depresible y no doloroso. Hepatomegalia de 4 cm sin esplenomegalia.
Ausencia de adenopatía en cuello, axilas o inglés.
Miembros inferiores sin edema, con pulsos pedios conservados.
Pruebas complementarias
Cardioscopia y eco pulmonar: Ventrículo izquierdo dilatado, no hipertrófico, con función sistólica severamente deprimida (FEVI Simpson 24%). Válvula aórtica trivalva, con buena apertura sin insuficiencia significativa. Válvula mitral con buena apertura e insuficiencia ligera. Ventrículo derecho ligeramente dilatado (DTD basal 40 mm), con función deprimida (TAPSE 13 mm). Insuficiencia tricuspídea grado 2, gradiente VD-AD 58 mmHg. VCI dilatada (24 mm), con colapso inspiratorio <50%. Derrame pleural bilateral, 1 EI, con colas de cometas hasta campos medios.
ECG (Figura 1): ECG: RS a 71 lpm. PR 150 ms. QRS: 86 ms. Onda T negativa asimétrica en V4 a V6.
Analítica de sangre: Hb 14 mg/dL, leucocitos 5500/μL, plaquetas 226000/μL,TP 11 s, TTPA 36,6s, fibrinógeno >500 mg/dL, creatinina 1,16 mg/dL, Ferritina 30 ng/mL, IST 12%, NT-ProBNP 10715 pg/mL.
Tratamiento y evolución
Se inicia tratamiento con triple terapia de bloqueo neurohormonal (empagliflozina 10 mg, espironolactona 25mg y sacuvitrilo/valsartan 24/26 mg c/12), omitiéndose incialmente la administración de betabloqueantes, que se inician al tercer día de ingreso (bisoprolol 1,25 mg). Se administra una dosis única de 1 gr de hierro carboxi-maltosa intravenoso y se mantiene el tratamiento domiciliario con sertralina 100 mg.
Al segundo día de ingreso se realiza PCR de Covid-19 debido a que enfermería refería tos frecuente, que la paciente minimizaba. El test es positivo, y la paciente confiesa que sabía que había parecido esta infección la semana previa, pero que la clínica había sido banal y que ya se consideraba curada. En la historia clínica consta pauta vacunal completa (3 dosis).
La paciente responde adecuadamente al tratamiento iniciado, con abundante diuresis de aproximadamente 3 L en las primeras 24 h y 2 L los dos días siguientes, por lo que se cambia el tratamiento diurético a furosemida oral.
La analítica mejora, con descenso de los niveles de NT-BNP a 2400 pg/mL al tercer día y solo un leve repunte de la creatinina, que asciende hasta 1,49 mg/dL.
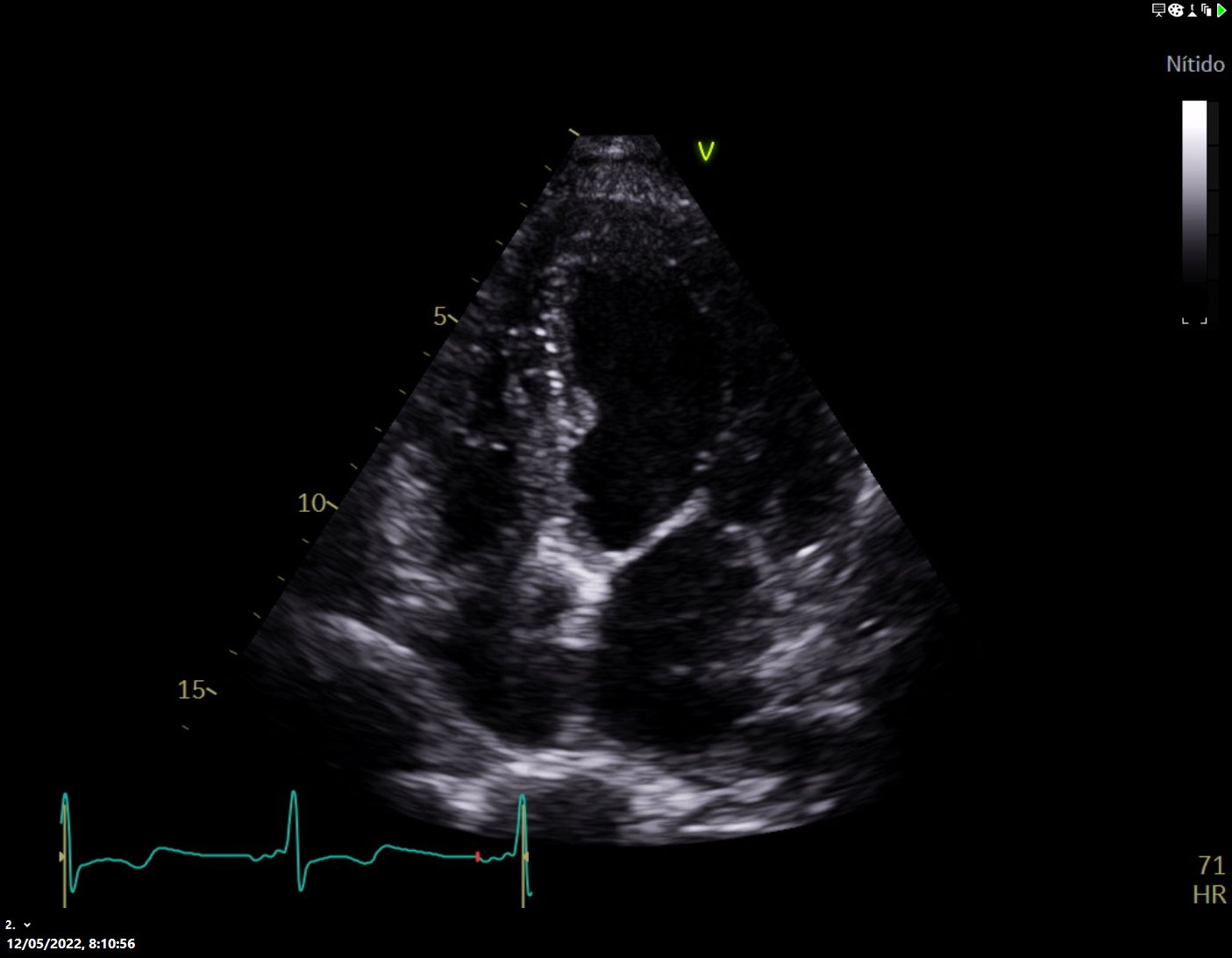
Al tercer día, ya con la auscultación pulmonar normalizada y habiendo desaparecido la disnea, se realiza ecocardiograma transtorácico reglado (Figura 2), en el que se evidencia ventrículo izquierdo ligeramente dilatado con FEVI moderadamente deprimida (FEVI 39%). Insuficiencia mitral mínima. Ventrículo derecho no dilatado, TAPSE 13 mm. Insuficiencia tricuspídea mínima, gradiente ventrículo derecho-aurícula derecha de 32mmHg.
Los días 4 y 5 no se realiza visita por no ser días laborables, pero la paciente permanece estable.
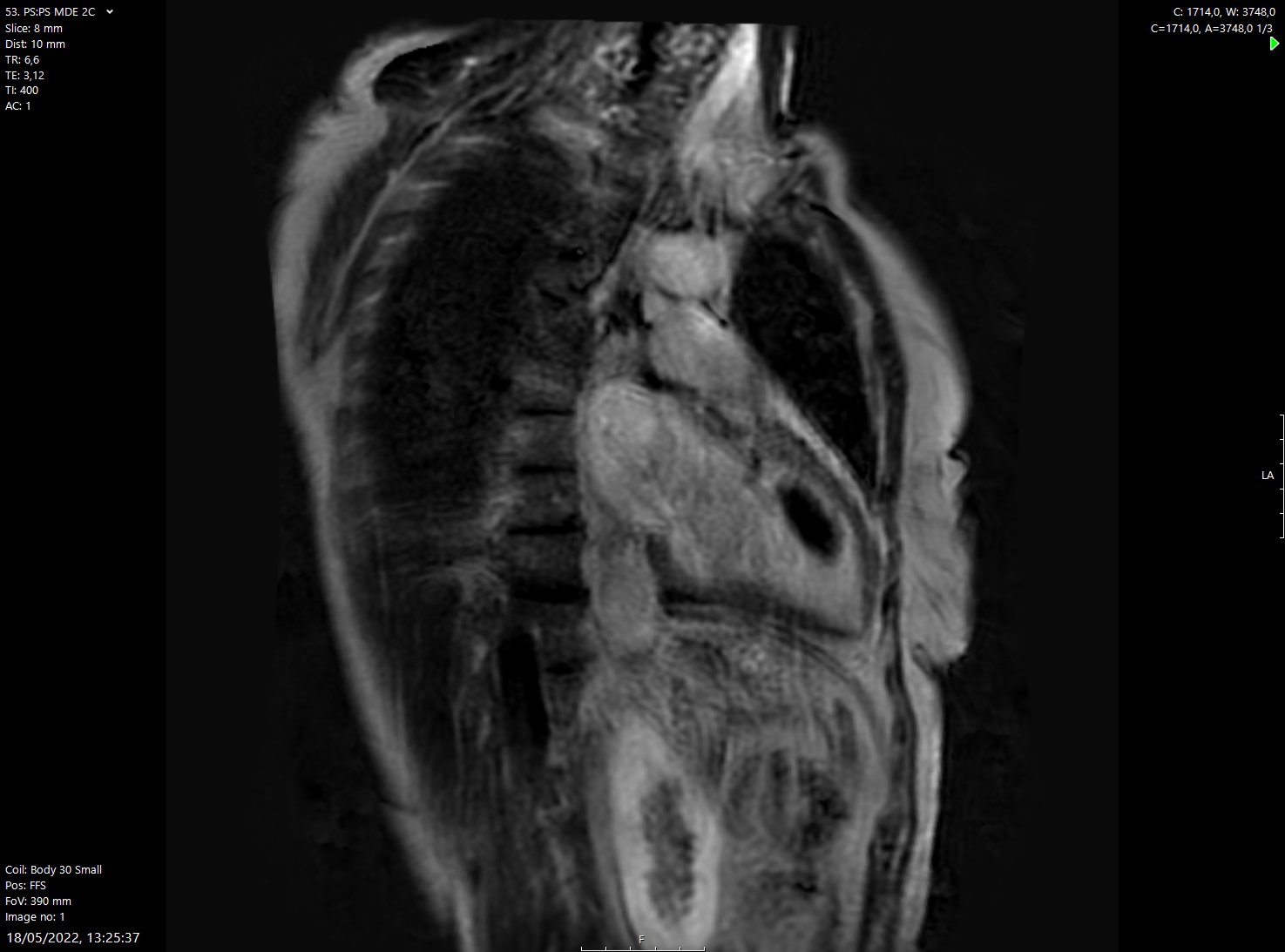
El día 6 se realiza cardio-RMN (Figura 3) para estudiar la etiología de la disfunción ventricular, remitiéndose el siguiente informe: Ventrículo izquierdo ligeramente dilatado, FEVI 24%. Ventrículo derecho no dilatado con función sistólica reducida (FEVD 42%). Gran trombo móvil en cavidad de VI de 38x22x20mm, adyacente a segmento medio de pared anterior, posiblemente agudo de acuerdo con caracterización tisular. Hallazgos compatibles con miocardiopatía dilatada. Dada la ausencia de realce tardío no se puede orientar hacia un origen determinado.
Lesiones esplénicas que requerirán de TC tóraco-abdominal para mejor caracterización.
Tras conocer dicha información se solicita, de acuerdo con hematología, se inicia anticoagulación con heparina no fraccionada, se pautan 20 mg c/6h de metilprednisolona oral y se solicita estudio de síndrome antifosfolípido y de autoinmunidad, con anticuerpos antinucleares, anticuerpos nucleares extraíbles y proteinograma. Además, se solicita TC toraco-abdómino-pélvico con contraste.
Asimismo, aunque la paciente comenta buen estado general, la familia afirmaba que desde hace dos días la veían ligeramente desorientada y con olvidos frecuentes, por lo que interconsultamos a neurología, realizamos exploración neurológica (que es anodina) y solicitamos TC craneal.
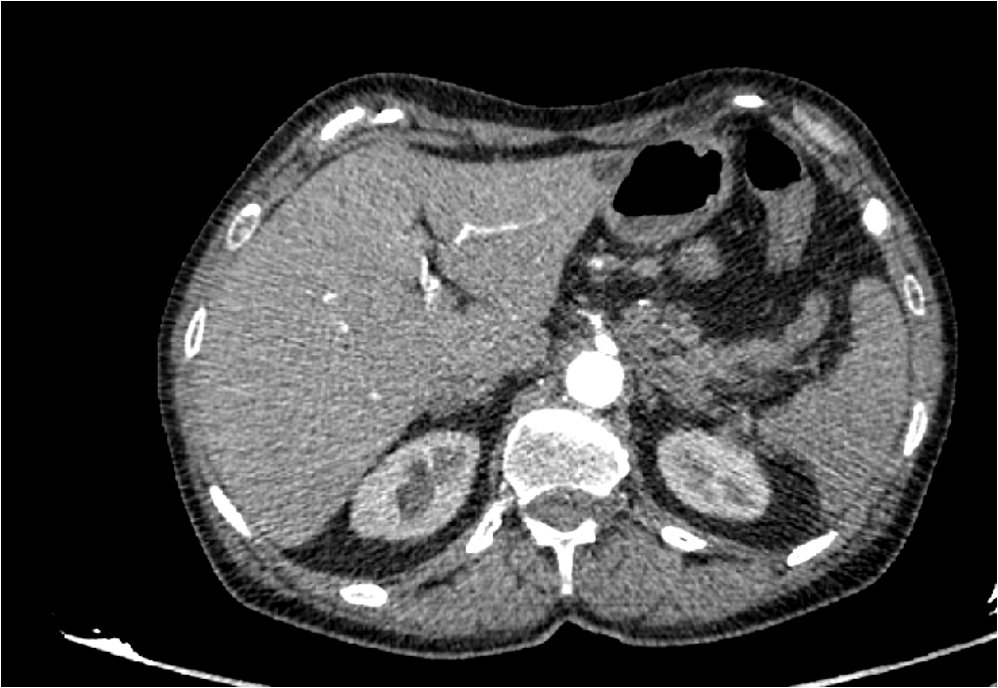
El TC tóraco-abdomino-pélvico con contraste (Figura 4) muestra trombosis aguda de la arteria y la vena esplénicas con infarto esplénico masivo.
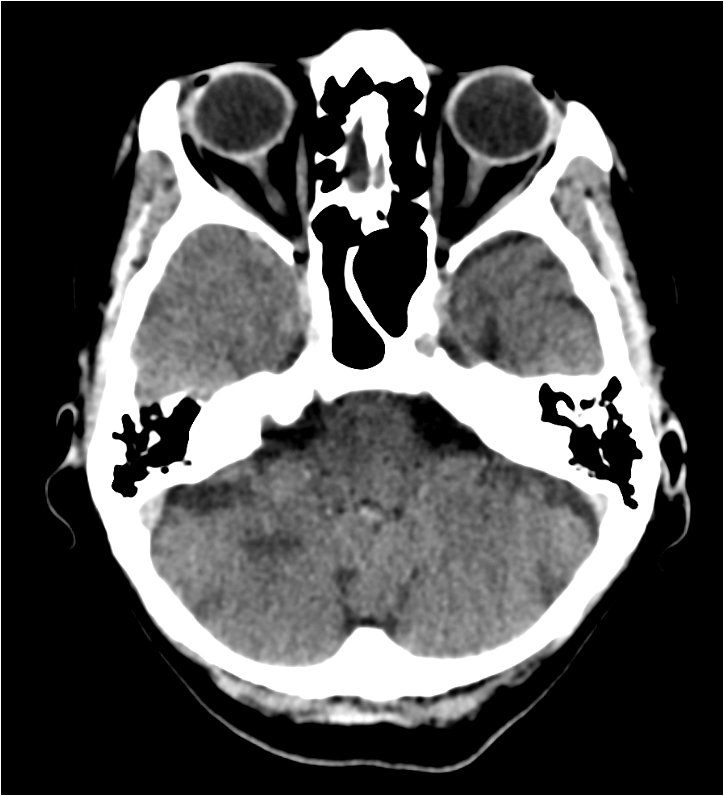
El TC craneal (Figura 5) muestra TAC craneal: Pequeña lesión hipodensa en hemisferio cerebeloso derecho que podría estar en relación con lesión isquémica reciente/subaguda. Se recomienda RMN cerebral.
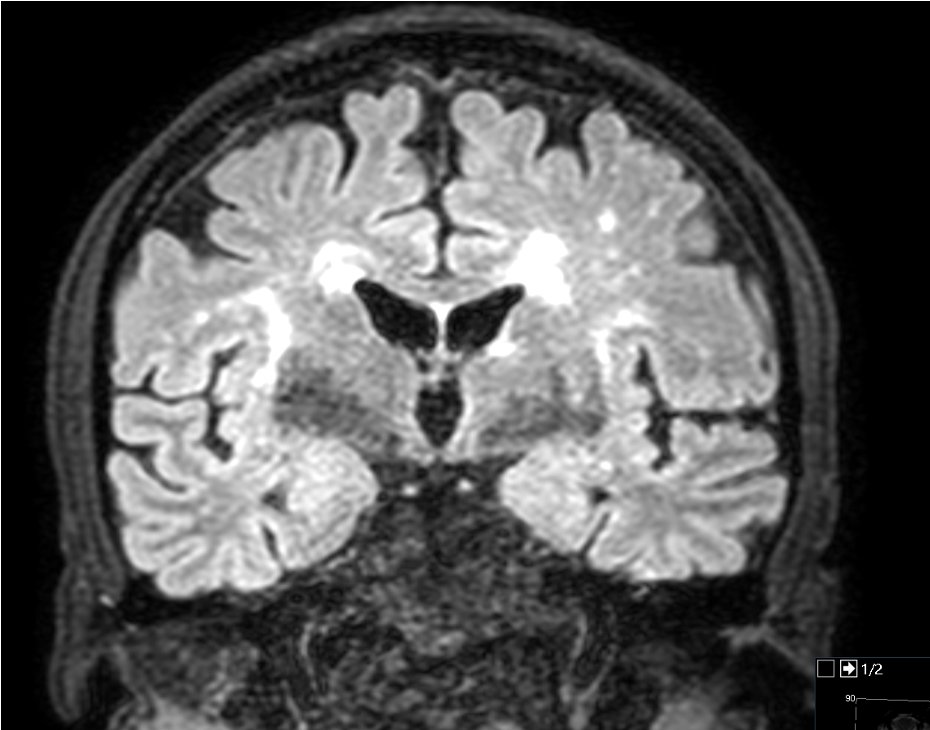
La RMN cerebral (Figura 6) muestra múltiples lesiones de pequeño tamaño y distribución parcheada, de origen isquémico reciente, en diferentes fases evolutivas.
Antes estos hallazgos y ante la ausencia de disminución del tamaño del trombo tras tres días de tratamiento anticoagulante, se decide intervención quirúrgica bajo circulación extracorpórea de forma emergente. La cirugía es exitosa, la anatomía patológica confirma la naturaleza tormbótica de la masa y la paciente se recupera de la misma favorablemente, sin más secuela que una fibrilación auricular paroxística postoperatoria cardiovertida con amiodarona y un bloqueo de rama izquierda del haz de Hiss.
Los estudios de autoinmunidad y de síndrome antifosfolípido son negativos.
La paciente se alta y se continúa seguimiento ambulatorio con cuádruple terapia para la insuficiencia cardíaca, anticoagulación con acenocumarol y pauta descendente de corticoides.
No presenta nuevos trombos intraventriculares y la FEVI se recupera parcialmente, siendo actualmente del 42%.
Discusión
El 9% de los pacientes que reciben tratamiento con antraciclinas desarrollan disfunción cardíaca durante el seguimiento3, y este riesgo aumenta a medida que aumenta la dosis total administrada. Aunque se sabe que puede existir un decalaje de varios años entre el fin del tratamiento y la detección de la disfunción ventricular, los estudios más recientes indican que el 98% de los casos se pueden detectar durante el primer año4. Pese a esto, nuestro caso evidencia que la cardiotoxicidad tardía no debe ser olvidada, subrayando así la importancia de una buena historia clínica.
En cuanto a la infección por coronavirus-19, podemos concluir de nuestro caso que, pese a la reducción de la mortalidad y de las complicaciones alcanzado con la vacunación, esta patología no es superponible a la gripe estacional o al resfriado común, y debemos recordar su asociación con fenómenos protrombóticos, incluso en pacientes sin otros estados procoagulantes identificados.
Finalmente, en lo que se refiere al manejo de los trombos interventriculares, todavía carecemos de estudios aleatorizados que aclaren cómo proceder cuándo su evolución es tórpida pese a la anticoagulación inicial, los cuales serían muy útiles antes de tomar una decisión tan trascendental como la indicación de una cirugía cardíaca emergente.
Bibliografía:
2. Levine GN, McEvoy JW, Fang JC, Ibeh C, McCarthy CP, Misra A, et al. Management of Patients at Risk for and With Left Ventricular Thrombus: A Scientific Statement From the American Heart Association. Circulation. 2022 Oct 11;146(15):e205-e223.
3. Lee JM, Park JJ, Jung HW, Cho YS, Oh IY, Yoon CH, et al. Left ventricular thrombus and subsequent thromboembolism, comparison of anticoagulation, surgical removal, and antiplatelet agents. J Atheroscler Thromb. 2013;20(1):73-93.
4. Lyon AR, López-Fernández T, Couch LS, Asteggiano R, Aznar MC, Bergler-Klein J, et al. 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS). Eur Heart J. 2022 Nov 1;43(41):4229-361.
5. Tran DB, AlAshi AK, Hernandez A. Delayed Onset Anthracycline-Associated Cardiotoxicity Presenting as Acute Decompensated Heart Failure Seven Years After Chemotherapy Completion. Cureus. 2021 Aug;13(8):e16920.